Patsiendile
Varia
Registreerimine
Registreerimine
eriarsti vastuvõtule
(vajalik isikukood)
1) Tel 731 9100
(E-R 07.30-18.00)
2) internetis Kliinikumi broneerimisvormi kaudu
3) Kliinikumi patsiendiportaalis
Vastuvõtuaega saab tühistada telefonil 731 9099
Kliinikumi üldinfo
E-P kell 08.00 – 19.00
Kontaktandmed
SA Tartu Ülikooli Kliinikum
Hematoloogia-onkoloogia kliinik
Puusepa 8,
50406 TARTU
Tel: +372 731 9802
Fax: +372 731 9804
e-post: ho@kliinikum.ee
Lümfoomid lastel
Laste kasvajatest on lümfoomid sageduselt kolmandal kohal leukeemiate ja ajukasvajate järel.
Tegemist on lümfisüsteemi kasvajaga, mis avaldub lümfisõlmede suurenemisena erinevates kehapiirkondades.
Sümptomid:
Lümfoomide kõige levinumaks tunnuseks on suurenenud lümfisõlmed, mis reeglina on valutud, tihked ja seotud neid ümbritsevate kudedega. Suurenenud lümfisõlme võib leida kaelal, kaenlaalusi, kubemes, lisaks rindkere- või kõhuõõnes. Haiguse edasiarenedes võivad kasvajalised lümfotsüüdid levida luuüdisse ja seljaaju vedelikku ehk liikvorisse.
Tüüpilisteks kaebusteks on väsimus, isutus, peavalu, kaalulangus, palavik, öised higistamised ja nahasügelus.
Diagnoos:
Diagnoosi saame, kui suurenenud lümfisõlm operatiivselt eemaldada ja selle ehitust mikroskoopiliselt uurida. Lümfisõlme eemaldamine toimub üldnarkoosis lastekirurgi poolt.
Kui lümfisõlmed on suurenenud ainult rinnakorvi sees või kõhuõõnes, siis tuleb proovitüki saamiseks ja haiguse täpseks diagnoosimiseks ette võtta suurem kirurgiline vahelesegamine.
Lümfoomide jaotus:
Histoloogilise leiu alusel jagunevad lümfoomid Hodgkini ja mitte-Hodgkini lümfoomideks. Esimesed on rohkem vanematel lastel - eelkõige puberteedieas ja teised väikelastel.
Hodgkini lümfoom erineb teistest lümfoomitüüpidest temas esineva ainult sellele haigusele omase rakutüübi poolest. Neid rakke nimetatakse tema avastajate järgi Reed-Sternbergi rakkudeks. Lümfisõlmed on suurenenud enamasti kaelal ja rindkeres.
Kasvaja mikroskoopilise ehituse alusel jaotatakse Hodgkini lümfoomid neljaks alatüübiks:
- nodullaarne skleroos
- segarakuline
- lümfotsüütide liiaga
- lümfotsüütide vaene
Diagnoosimisel jaotatakse haiged riskigruppidesse, sõltuvalt haiguse ulatusest: madal-, kesk- ja kõrgrisk. See on aluseks raviskeemi valikul.
Mitte-Hodgkini lümfoomid moodustavad lapseea lümfoomidest 60%. Lümfoom võib alguse saada nii B- kui ka T-lümfotsüütidest.
Vastavalt kasvaja mikroskoopilisele ehitusele jaotatakse haigus alatüüpidesse:
- Burkitt lümfoom
- T-lümfoblastne lümfoom
- Difuusne suur-rakk lümfoom
- Suurrakk anaplastne lümfoom
Staadiumid:
Haiguse ulatuse hindamiseks tuleb kasutada erinevaid röntgenoloogilisi uurimismeetodeid:
rindkere röntgen, kompuutertomograafiline (KT) või positron emission tomograafiline (PET) uuring. Lisaks luuüdi punktsioon, et hinnata kas haigus on haaranud luuüdi ning lumbaalpunktsioon, et hinnata kas haigus on levinud kesknärvisüsteemi.
Vastavalt kasvajast haaratud piirkondade arvule ja paiknemisele jaotatakse nii Hodgkini kui mitte-Hodgkini lümfoomid nelja staadiumi. Kui haigel esineb palavik, öised higistamised või kaalulangus, siis lisatakse staadiumile B täht, nende sümptomite puudumisel aga A täht.
Ravi
Lümfoomide raviks kasutatakse tsütostaatilisi ravimeid ehk keemiaravimeid ja kiiritusravi. Raviskeemi valik, ravimite hulk, ravi kestvus ja ravimite doosid sõltuvad lapse vanusest, kasvaja histoloogilisest tüübist, suurusest ja levikust.
Hodgkini lümfoomi ravi sõltub haiguse riskigrupist:
kasutatakse erinevaid raviskeeme
- OEPA (vinkristiin, etoposiid, prednisoloon, doksorubitsiin;) poistele
- OPPA (vinkristiin, prokarbasiin, prednisoloon, doksorubitsiin), tüdrukutele
- COPP tsüklofosfamiid, vinkristiin, prokarbasiin, prednisoloon)
- ABVD (doksorubitsiin, bleomütsiin, vinblastiin, dakarbasiin)
- BEACOPP (bleomütsiin, etoposid, doksorubitsiin, tsüklofosfamiid, vinkristiin, prednisolon, prokarbasiin)
Kiiritusravi teostatakse sõltuvalt keemiaravi poolt saadud ravivastusest.
Mitte-Hodgkini lümfoomide ravi sõltub histoloogilisest alatüübist:
- T rakuline prekursor lümfoblastne lümfoom: NOPHO ALL-08 HR raviskeem
- Burkitt lümfoom: LMB2001 või BFM NHL-04 raviskeem
- Difuusne B suur-rakklümfoom: EURO-LB 02 raviskeem
- Anablastne suurerakuline lümfoom: ALCL-99 raviskeem
Ravi ajal ja järgselt teostatakse uuringud hindamaks ravi efektiivsust. Üldiselt taluvad lapsed keemiaravi hästi. Probleemiks on keemiaravijärgne leukopeenia periood, kus esinevad infektsioonid, mille tõttu peab jälle haiglas olema.
Kui haigus ei allu esmaravil, on näidustatud kõrgdoosis keemiaravi koos vereloome tüvirakkude siirdamisega.
Lümfoomid alluvad reeglina ravile hästi. . Hodkini lümfoomide korral on 5 aasta elulemus >90% ja mitte-Hodgkini lümfoomide korral, mis on agressiivsemad, on elulemus >70%.
Ajukasvajad lastel
Ajukasvajad on lastel sageduselt leukeemiate järel 2. kohal.
Kasvajate jaotus
Healoomulised ajukasvajad ei sisalda vähirakke, kasvaja rakud ei tungi ümbritsevatesse kudedesse ega levi keha teistesse osadesse.
Pahaloomulised ajukasvajad sisaldavad vähirakke, on kiire kasvuga ja tungivad ümbritsevasse tervesse ajukoesse või avaldavad sellele survet. Vähi levimist kutsutakse siirete tekkimiseks ehk metastaseerumiseks.
Vaatamata sellele, kas tegemist on healoomuliste või pahaloomuliste rakkude vohamisega, kujutavad ajukasvajad alati suurt ohtu, sest iga kasvaja avaldab vastavalt oma paiknemisele rõhku ajukoele.
Sümptomid:
Laste ajukasvajatest suurim osa paikneb kas keskjoonel, tõkestades liikvori ringet ja põhjustades koljusisese rõhu tõusu või tagumises koljukoopas, tekitades seal paiknevate ajuosade funktsiooni häireid. Sümptomideks on peavalu, mis pidevalt süveneb ning avaldub hommikul või äratab öösel, peamiselt tekib lamamisel. Peavaluga kaasneb iiveldus ja oksendamine ning valule mõjub halvendavalt rõhu tõus (köhimine, pingutus). Lisaks võivad esineda kahelinägemine, tagumises koljukoopas olevate kasvajate korral tasakaaluhäired, kohmakus ja halvatusnähud.
Diagnoosimine:
Kui neuroloogilisel uuringul esineb patoloogiline leid või anamneesi alusel tekib ajukasvaja kahtlus, tuleks teostada aju piltdiagnostika: pea kompuutertomograafia või magnetresonantstomograafia - uuringud, mis annavad ülevaate peaajus esinevatest ehituslikest muutustest. Kui nende uuringute alusel on kahtlus kasvajale, siis neurokirurg operatiivsel teel eemaldab kasvaja kas täielikult või osaliselt ja patoloog annab histoloogilise vastuse. Haiguse ulatuse hindamiseks vajalik ka seljaajuvedeliku ehk liikvori uuring.
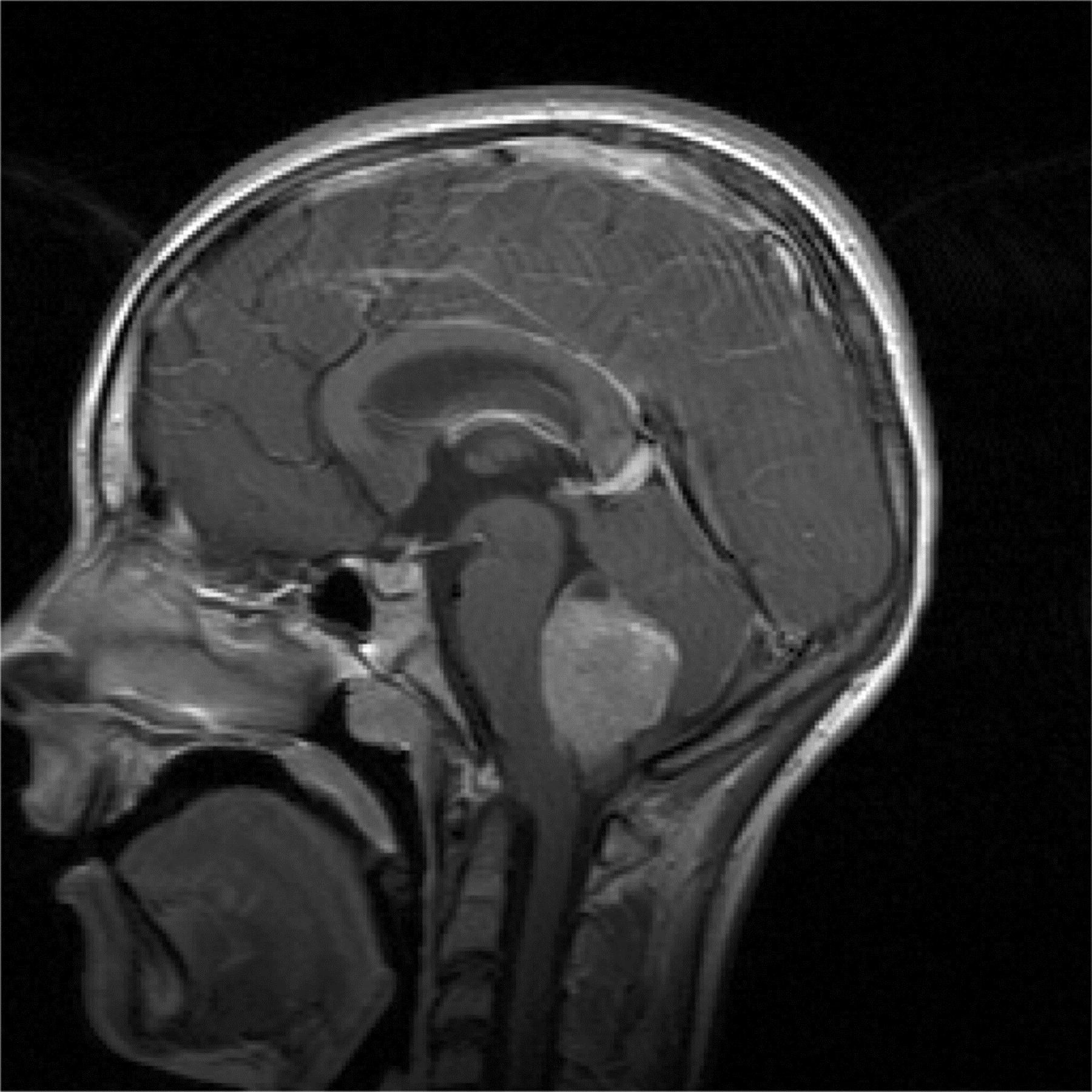
Sagedasemad kasvajad:
Madalmaliigsed glioomid moodustavad 40% lapseea ajukasvajatest. Glioome iseloomustatakse täiendavalt selle alusel, mis tüüpi rakke nad haaravad: astrotsütoom lähtub tähekujulistest gliiarakkudest, mida kutsutakse astrotsüütideks. Kõige sagedasem alatüüp on pilotsüütastrotsütoom, mis on aeglase kasvuga. Kõige tavalisem vanuses 3-14.aastat. Sagedaseim pahaloomuline kasvaja lastel on medulloblastoom, moodustades 20% ajukasvajatest. See kasvaja lähtub tavaliselt väikeajust. Keskmise vanus diagnoosimisel on 5.- 9. aastat. Peale operatsiooni jaotatakse haiged riskigruppidesse.
Ependümoom lähtub rakkudest, mis vooderdavad vatsakesi või seljaaju keskkanalit, moodustades 10% ajukasvajatest. Keskmine vanus diagnoosimisel esimesed neli eluaastat.
Ravi:
Ravi valik sõltub kasaja histoloogiliselt tüübist, kasvaja lokalisatsioonist, ulatusest ja lapse vanusest diagnoosimisel. Rakendatakse kas kirurgilist- , kiiritus- või keemiaravi.
Opereerimine oleneb eelkõige kasvaja asukohast, nt. ajutüves, nägemisnärvide ja kõnekeskuse piirkonnas olevaid kasvajaid ei saa operatiivselt eemaldada. Osa opereerimatuid kasvajaid põhjustab hüdrotsefaaliat ehk vesipead ning sellisel juhul võib abi saada šunteerimisest - seljaajuvedeliku normaalse ringe taastamisest vastava nö. torude süsteemiga.
Suure osa healoomuliste ajukasvajate täieliku eemaldamise järgselt paraneb laps täielikult.
Keemiaravi on põhiline ravivalik operatsiooni järgselt väikelastel. Medulloblastoomi korral kasutatakse HIT 2000 imikute raviprotokolli.
Pilotsütaarse astrotsütoomi korral esmavalikuks on tuumori operatiivne eemaldamine ja lapse jälgimine. Kui asukoha järgi ei ole võimalik kasvajat eemaldada, siis järgneb keemiaravi: vinkristiin ja karboplatiin 4. nädalaste vahedega aasta jooksul.
Kiiritusravi kuulub raviskeemi suurematel lastel.
Medulloblastoomi korral üle 4 aastastel lastel operatsiooni järgselt kiiritusravi, mille ajal manustatakse kord nädalas vinkristiini veenisiseselt. 6 nädalat peale kiiritusravi järgneb keemiaravi: lomustiin, tsisplatiin, vinkristiin, kokku 8. kuuri 6 nädalaste intervallidega.
5 aasta elulemus standardriski korral 85%, kõrgriski korral>60%.
Ependümoomi korral üle 3.a. lastel järgneb tuumori operatiivsele eemaldamisele kiiritusravi.
Ajukasvajaga haiget tuleb pidevalt jälgida. Sõltuvalt kasvaja iseloomust on kontrolluuringud kas 3. või 6.kuuliste intervallidega 5 aasta jooksul peale ravi lõppemist.
Ka pärast operatsiooni ja kiiritusravi on võimalik, et kasvaja hakkab uuesti vohama, tekib nn. retsidiiv. Retsidiivi võib oletada, kui lapsel neuroloogilised sümptomid halvenevad, epilepsiahood sagenevad või on varasematest erinevad, süveneb väsimus, laps oksendab ja kaebab peavalu.
Omandatud trombotsüütide funktsioonihäired
Haigused või nendega seoses olevad seisundid võivad mõjutada trombotsüütide normaalset talitlust, mille tagajärjeks on omandatud trombotsüütide funktsioonihäire teke.
Põhjused, esinemissagedus ja riskifaktorid
Trombotsüüdid ehk vereliistakud on vererakud, mis on hädavajalikud vere hüübimiseks.
Trombotsüütidega seotud hüübimishäired võivad olla tingitud kas liiga vähesest või liiga rohkest vereliistakute hulgast. Ka normaalse trombotsüütide arvu korral võib vere hüübimine olla häiritud, kuna vereliistakud ei funktsioneeri korralikult.
Trombotsüütide funktsioonihäireid põhjustavad nii pärilikud haigused kui ka omandatud seisundid. Paljudel juhtudel võib trombotsüütide arv olla normis või isegi suurenenud, kuid ikkagi esineb veritsus. Trombotsüütide funktsioonihäireid põhjustavad näiteks müeloproliferatiivsed haigused (essentsiaalne trombotsüteemia, tõeline polütsüteemia), neerupuudulikkus, müeloomtõbi, leukeemiad ning sellised ravimid nagu aspiriin ja teised mittesteroidsed põletikuvastased ravimid (indometatsiin, ibuprofeen, naprokseen), tiklopidiin, klopidogreel, hepariin, varfariin, mõned antibiootikumid, südameravimid, antidepressandid ja allergiavastased preparaadid. Trombotsüütide funktsioon taastub, kui nende ravimite võtmine lõpetada.
Vältimine
Ettevaatlikkus ravimite tarvitamisel võib vähendada ravimitega seotud omandatud trombotsüütide funktsiooni defekte. Teiste haiguste ravi vähendab samuti hüübimishäire tekkeriski.
Sümptomid
• Ninaveritsus
• Igemete veritsus
• Kergesti tekkivad nahaalused verevalumid
• Vererohked menstruaalverejooksud
• Pikaleveniv menstruaalveritsus
Diagnoosimine
Veritsussümptomite esinemisel tehakse mitmeid hüübimissüsteemi uuringuid.
• Pikenenud veritsusaeg
• Ebanormaalne trombotsüütide agregatsiooni test
• Normaalne, kõrge või madal trombotsüütide arv
Ravi
Ravi on suunatud trombotsüütide funktsioonihäiret põhjustava seisundi korrigeerimisele. Kui on tegemist neerupuudulikkusega, vähendab veritsust dialüüs. Vajalikuks võib osutuda trombotsüütide ülekanne või trombaferees müeloproliferatiivsete haiguste korral.
Nina- ja igemeveritsuse raviks sobib antifibrinolüütiline ravi (traneksaamhape). Osadel juhtudel on kasu desmopressiini manustamisest. Suurt verekaotust menstruatsioonide korral saab vähendada suukaudsete rasestumisvastaste tablettide ja antifibrinolüütilise preparaadiga.
Prognoos
Defekti korrigeerib tavaliselt trombotsüütide funktsioonihäiret põhjustanud seisundi ravi.
Aplastiline aneemia
Aplastiline aneemia (AA) on harvaesinev haigus, mille puhul luuüdi ei ole võimeline tootma piisaval hulgal vereloome rakke.
Põhjused, esinemissagedus, riskifaktorid
Aplastiline aneemia on seisund, mille põhjuseks on vereloome tüviraku kahjustus, mille tulemusena on vähenenud kõikide vereloome rakkude – erütrotsüütide, leukotsüütide, trombotsüütide hulgad ja tekib nn pantsütopeenia. Tüvirakk on eellasrakuks kõikidele teistele vereloome rakkudele. Tänapäeval arvatakse, et enamasti on AA puhul tegemist autoimmuunse protsessiga, mis tähendab, et patsiendi enda immuunsüsteem reageerib omaenda tüvirakkude vastu. Kuni 70-80% juhtumitest kindel haigusetekke põhjus pole teada. Sellist AA nimetatakse idiopaatiliseks.
Teatud keskkonna tegurid võivad olla samuti seotud AA tekkega. Nende hulka kuuluvad erinevad ravimid, kemikaalid, toksiinid, viirushepatiit. Harva on tegemist kaasasündinud haigusseisunditega, millele on samuti iseloomulik aplastiline aneemia. AA esinemissagedus maailmas on 2 juhtu 1 000 000 elaniku kohta aastas. Haiguse ennetamise meetmeid ei ole teada.
Haiguse sümptomid
Sümptomid on tingitud tsirkuleerivate vererakkude arvu langusest ning ei ole haiguse spetsiifilised. Sarnased sümptomid võivad esineda näiteks ägeda leukeemia või müelodüsplastilise sündroomi puhul, mis tõttu algul võivad arstid kahtlustada muud verehaigust.
Aneemia põhjustab väsimus- ja nõrkustunnet. Patsient võib märgata, et ta väsib kiiresti ära juba minimaalse füüsilise koormuse puhul. Nahk muutub kahvatuks. Valgevererakkude vähesus põhjustab infektsioonide riski suurenemist. Trombotsütopeenia võib tüsistuda veritsusega.
Sagedamini esinevad sümptomid on :
- Väsimus, jõuetus
- Kahvatus
- Hingeldus
- Südamepekslemine
- Ninaveritsused, igemete veritsused
- Verevalumid nahal, limaskestadel
- Palavik
Haiguse diagnoosimine
Diagnoosi kinnitamiseks on vajalikud vere- ja luuüdi uuringud. Vereproov näitab, et kõikide rakkude arv on normist madalam. Erinevalt mõnest teisest verehaigusest ei leidu aga veres atüüpilisi rakke. Diagnoosi kinnitamiseks on vajalikud luuüdi morfoloogilised uuringud, milleks materjali saadakse luuüdi punktsioonil, mis teostatakse lokaalse tuimestusega.
Ravi
Ravi võib jagada kaheks suureks rühmaks. Toetava ravi puhul on oluline asendada neid vererakke, mida on organismis vähe. Selleks tehakse erütrotsüütide ja trombotsüütide ülekandeid ning hoitakse ära aneemiaga ja trombotsütopeeniaga seotud tüsistusi. Lisaks on oluline vältida infektsioone, milleks kasutatakse profülaktilisi meetmeid, kaasa arvatud profülaktiline antibakteriaalne ravi. Vahest piirdutaksegi ainult toetava raviga.
Teiseks ravivõimaluseks on üritada taastada luuüdi normaalset funktsioneerimist. Noortele inimestele on näidustatud allogeenne ehk sobiliku doonorluuüdi siirdamine. Parimaks võimalikuks doonoriks on patsiendi enda õed – vennad, kuid tõenäosus , et nende luuüdi sobib patsiendile on umbes ¼. Võimalik ka luuüdi siirdamine mittesugulasdoonorilt. Luuüdi siirdamisega seotud probleemideks on eeskätt infektsioonid, äratõukereaktsiooni risk ning ka siiriku reaktsioon peremehe vastu (nn transplantaat peremehe vastane reaktsioon, ingl keeles graft-versus-host; GVH). Enne siirdamist tehakse keemiaravi, mis on nn ettevalmistus protseduuriks.
Juhul, kui siirdamine pole mingil põhjusel võimalik (ei leidu sobivat doonorit, patsiendi üldseisund ei võimalda protseduuri jne), siis kasutatakse medikamentoosset ravi. Medikamentoosset ravi võib kasutada ka enne siirdamist. Selle ravi eesmärgiks on suruda maha organismi enda immuunsüsteem, mis võimaldab luuüdil taastada rakkude produktsioonivõime.
Sagedamini kasutatav medikamentoosne ravi:
- ATG e. antitümotsütaarne globuliin - valk (globuliin), mis sisaldab T-lümfotsüütide vastaseid antikehi ning mida kasutatakse eesmärgil suruda maha organismi enda immuunsüsteem. Sageli kasutatakse kombinatsioonis tsüklosporiiniga. ATG ravi eripäraks on see , et efektiivsust enamasti saab hinnata alles 3-4 kuu pärast. Kuni 70% juhtumitest on ravi efektiivne. Mõnikord tekib vajadus teha ravikuure korduvalt.
- Tsüklosporiin – ravim, mis samuti mõjutab organismi immuunsüsteemi. Kasutatakse kombinatsioonis ATG-ga või monoteraapiana. Ravi on enamasti pikaajaline.
- Harvemini kasutatakse muid ravimeid, nt kortikosteroide, androgeene, tsüklofosfamiidi. Tänapäeval kasutatakse üksikpreparaatidena neid harva.
Nagu ka muud ravimid, võivad AA korral kasutatavad ravimid põhjustada erinevaid kõrvaltoimeid. ATG kasutamisel võib tekkida allergiline reaktsioon. Tsüklosporiin võib kahjustada neerusid, maksa, mis tõttu on oluline kontrollida ravimi kontsentratsiooni veres. Ravivalik sõltub haiguse raskusest, raviga seotud riskidest ja kõrvaltoimetest ning patsiendi üldseisundist ja vanusest.
Prognoos
Aplastiline aneemia on progresseeruv haigus, mis ilma ravita on prognoositu. Ka saavutatud raviefekti puhul jääb risk, et haigus tuleb tagasi, mis tõttu olulisel kohal on regulaarne jälgimine ka siis, kui ravi on lõpetatud. Ravi eesmärgiks ei ole alati tervistumine. Oluline on parandada luuüdi funktsiooni ning vähendada vereülekannete vajadust ja infektsioonide riski. Luuüdi siirdamine noorematele inimestele (alla 30 aasta vanuses) on andnud häid tulemusi pikaajalise elulemusega kuni 80% juhtudest, vanematel inimestel 40-70% juhtudest.
Immuuntrombotsütopeenia
Immuuntrombotsütopeenia (ITP), tuntud ka idiopaatilise trombotsütopeenilise purpura nime all, on autoimmuunne haigus. Autoimmuunse haiguse esinemisel ei suuda immuunsüsteem enam vahet teha oma ja võõra vahel ning kujuneb välja immuunreaktsioon enese kudede vastu.ITP korral on märklauaks trombotsüüdid. Immuunsüsteemi poolt on need vererakud märgistatud kui võõrad ja kõrvaldatakse põrna, maksa poolt või mõnel muul moel. Lisaks trombotsüütide suurenenud lammutamisele võib olla häirunud trombotsüütide tootmine luuüdis.
Sümptomid
Väikese trombotsüütide arvu korral esinevad inimesel sageli veritsusnähud. Kergesti tekivad purpursed nahalused verevalumid, väikesed punased täppverevalumid, ninaveritsused, naistel võivad olla vererohked menstruatsioonid. Ohtlikumateks veritsussümptomiteks on verevalumid suus, veri uriinis või väljaheites, ajuverejooks.
Diagnoosimine
Normaalselt on trombotsüütide arv veres 145 – 400 x109/L. Kui trombotsüütide arv on alla 100 x109/L ning ei leita ühtegi teist trombotsütopeenia tekkepõhjust, diagnoositakse ITP.
Lastel eelneb immuuntrombotsütopeeniale sageli viirusinfektsioon ning paranemine võib toimuda ilma ravita 6-8 nädalaga. Täiskasvanutel on tavaliselt tegemist haiguse kroonilise kuluga, st haigus kestab üle poole aasta.
ITP esineb naistel sagedamini kui meestel ja lastel sagedamini kui täiskasvanutel. Riskifaktorid ei ole teada, seetõttu ei osata haigust ära hoida.
Haigestumus on 3-6 juhtu 100 000 elaniku kohta aastas.
Ravi
Haiguse ravi sõltub trombotsüütide arvust, veritsussümptomite raskusest, vanusest, elustiilist, inimese isiklikest ravieelistustest ja teistest põetavatest haigustest.
Tavaliselt alustatakse ravi prednisolooniga. Kiire trombotsüütide arvu paranemine on võimalik saavutada ka suures annuses immuunglobuliini veeni manustamisega. Lastele sobib korduv anti-D immuunglobuliini süstimine.
Kui haigus ei reageeri esialgsele ravile, võetakse kasutusele preparaadid, mis suruvad maha immuunsüsteemi aktiivsust (rituksimab, tsüklosporiin, tsüklofosfamiid) või soodustavad trombotsüütide tootmist luuüdis (romiplostiim, eltrombopag).
Splenektoomia ehk operatiivne põrna eemaldamine on näidustatud, kui muu ravi ei aita, haigus on kestnud pikemat aega, vere trombotsüütide tase on väga madal ning esinevad veritsused. Kuna trombotsüütide lammutamine toimub peamiselt põrnas, siis splenektoomia lahendab trombotsütopeenia probleemi enamusel inimestel.
Eluohtliku verejooksu puhul kasutatakse lisaks trombotsüütide ülekannet.
Veritsusnähte aitab vähendada traneksaamhape parandades vere hüübivust.
Inimesed, kellel on ITP, peaksid hoiduma aspiriini, ibuprofeeni ja diklofenaki kasutamisest, kuna need ravimid võivad soodustada veritsuse tekkimist. Planeeritavate hambaarsti külastuste ja kirurgiliste operatsioonide eelselt on soovitav nõu pidada hematoloogiga.
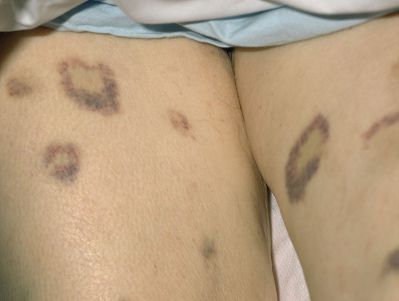
Naha purpur
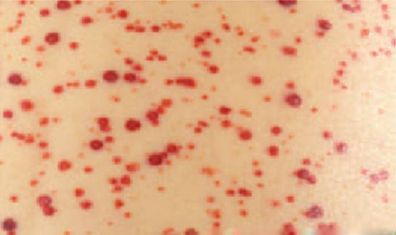
Täppverevalumid
